研究内容Research
研究テーマの概要
炎症制御の分子機構の解明
自然免疫系はToll-like receptor (TLR)を始めとした受容体によりウイルスや細菌など病原体の感染を直接認識し,サイトカインを産生,炎症を引き起こします(下図)。炎症は感染制御だけでは無く,自己免疫疾患や癌,メタボリックシンドロームなど様々な疾患と深く関わる事が明らかとなってきています。本研究分野では,自然免疫により引き起こされる炎症が生体内においてどのように制御されているかの分子メカニズムを遺伝子改変マウスを用いて解析しています。
現在,大別して以下の3つの研究プロジェクトを進めています。
- ウイルス,細菌感染に対する自然免疫機構の研究
- 炎症応答制御の分子機構に関する研究
- RNAを介した免疫制御に関する研究
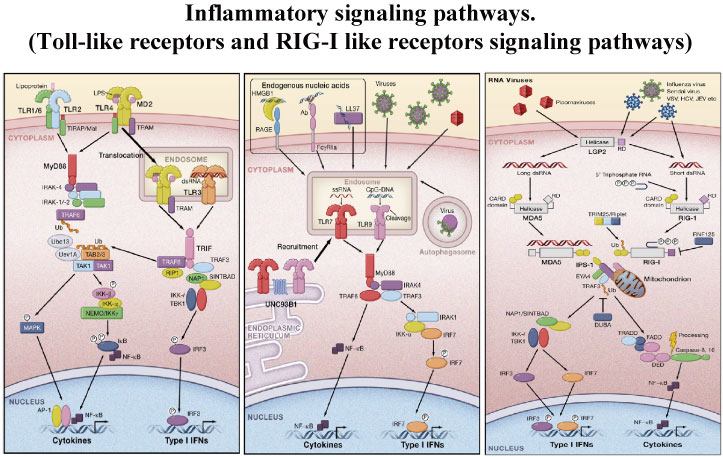
(Takeuchi, O., Akira, S. (2010). Pattern recognition receptors and inflammation. Cell 140, 805-820.)
1. ウイルス, 細菌感染に対する自然免疫機構の研究
ウイルスや細菌などの感染はToll-like receptor (TLR)やRIG-I-like receptor (RLR)などの自然免疫受容体により認識され,細胞内シグナル伝達経路活性化の結果,炎症性サイトカインが産生されます。私たちはこれまで,TLRやRLRの感染認識における役割を解析してきたほか,その細胞内シグナル伝達経路に関しても解析を加えてきました。現在,このシグナル伝達分子の生理機能に関しても遺伝子改変動物を用いて研究を行っています。
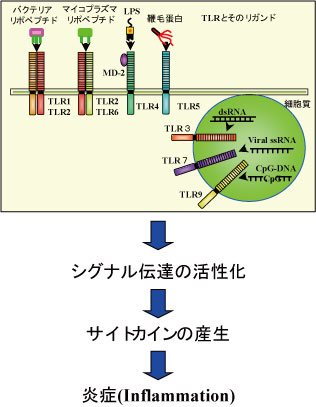
代表的な発表論文
- Tartey, S., Matsushita, K., Imamura, T., Wakabayashi, A., Ori, D., Mino, T., Takeuchi, O. (2015). Essential Function for the Nuclear Protein Akirin2 in B Cell Activation and Humoral Immune Responses. J. Immunol. 195, 519-527.
- Tartey, S., Matsushita, K., Vandenbon, A., Ori, D., Imamura, T., Mino, T., Standley, D.M., Hoffmann, J.A., Reichhart, J.M., Akira, S., Takeuchi, O. (2014). Akirin2 is critical for inducing inflammatory genes by bridging IκB-ζ and the SWI/SNF complex. EMBO J. 33, 2332-2348.
- Miyake, T., Satoh, T., Kato, H., Matsushit, K., Kumagai, Y., Vandenbon, A., Tani, T., Muta, T., Akira, S., Takeuchi, O. (2010). IκBζ is essential for natural killer cell activation in response to IL-12 and IL-18. Proc. Natl. Acad. Sci. USA 107, 17680-17685.
- *Satoh, T., *Takeuchi, O., Vandenbon, A., Yasuda, K., Tanaka, Y., Kumagai, Y., Miyake, T., Matsushita, K., Okazaki, T., Saitoh, T., Honma, K., Matsuyama, T., Yui, K., Tsujimura, T., Standley, D.M., Nakanishi, K., Nakai, K., Akira, S. (*Equal contribution). (2010). The Jmjd3-Irf4 axis regulates M2 macrophage polarization and host responses against helminth infection. Nat. Immunol. 11, 936-944.
- Takeuchi, O., Akira, S. (2010). Pattern recognition receptors and inflammation. Cell 140, 805-820.
- Satoh, T., Kato, H., Kumagai, Y., Yoneyama, M., Sato, S., Matsushita, K., Tsujimura, T., Fujita, T., Akira, S., Takeuchi, O. (2010). LGP2 is a positive regulator of RIG-I- and MDA5-mediated antiviral responses. Proc. Natl. Acad. Sci. USA 107, 1512-1517.
2. 炎症抑制分子メカニズムの解析
炎症性サイトカインの産生は炎症応答に重要ですが,この産生は生体内において精緻に調節されています。このバランスがくずれ,例えばサイトカインの産生が十分に起こらないと免疫不全症の原因になり,これに対し,サイトカインが過剰に産生されると,敗血症性ショックや自己免疫疾患などの原因となります。
この調節がどのように行われているかのメカニズムを炎症関連遺伝子発現の転写,転写後調節に焦点を当てて研究しています。
TLRシグナルを抑制する機構に関して検討を加え、アダプター分子であるTANKがTRAF6を介してTLRシグナルを抑制する役割を果たしていることを見いだしました。TANKを欠損するマウスではTLR刺激による転写因子NF-κBの活性化が亢進しIL-6を始めとしたサイトカインが非常に多く産生されるほか、IL-6依存性に自己免疫性糸球体腎炎を自然発症します。現在、TANKやそのファミリー分子の分子機能、自己免疫疾患発症のメカニズムに関し更に検討を加えています。
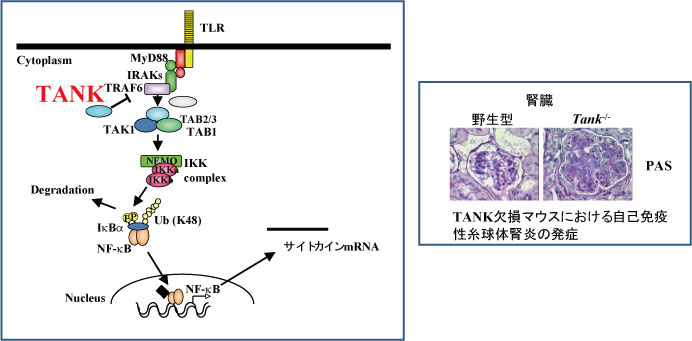
代表的な発表論文
- *Kawagoe, T., *Takeuchi, O., Takabatake, Y., Kato, H., Isaka, Y., Tsujimura, T., Akira, S. (*Equal contribution). (2009). TANK is a negative regulator of Toll-like receptor signaling and is critical for the prevention of autoimmune nephritis. Nat. Immunol. 10, 965-972.
3. RNAを介した免疫制御に関する研究
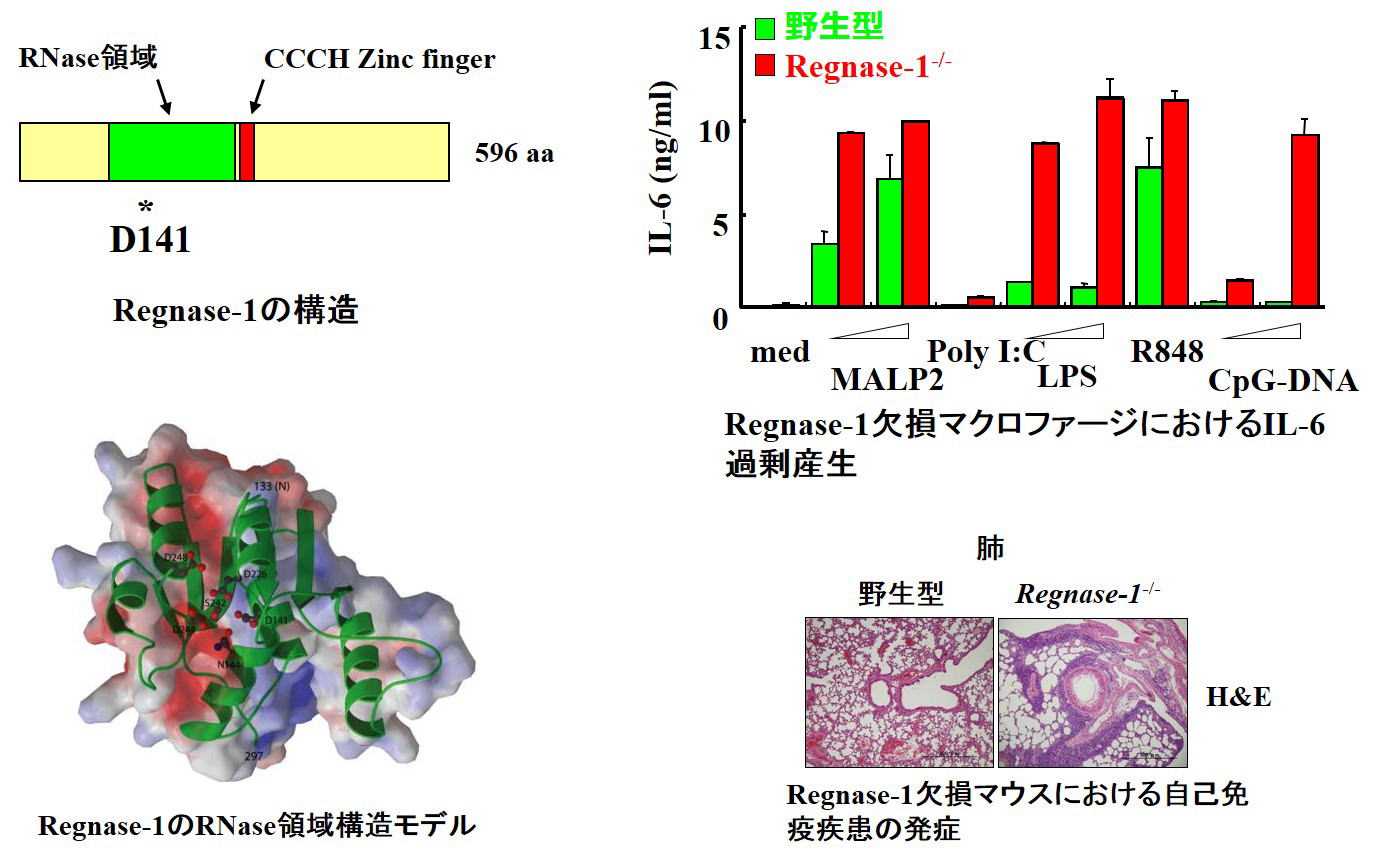
私たちはIL-6を始めとしたサイトカインmRNAの分解に関わるRNA分解酵素Regnase-1 (Zc3h12a, Mcpip1)を同定し,この分子の遺伝子欠損マウスを作製,解析することにより,Regnase-1が自己免疫性炎症性疾患の発症抑制に重要であることを明らかにしました(PubMed)。
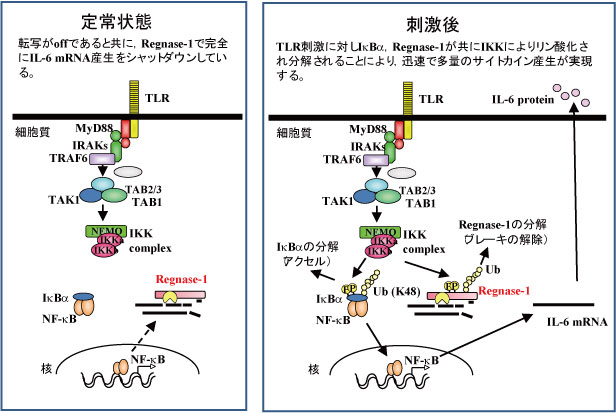
また,Regnase-1タンパク質はTLRシグナルによりリン酸化,分解されることで一時的にそのブレーキを外し,サイトカイン産生を誘導している事を解明しました(下図,PubMed)。
更に,Regnase-1は,自然免疫細胞だけでなく,T細胞においてc-Rel,OX40,IL-2などのmRNAを分解することで,T細胞の活性化を抑制する重要なRNA分解酵素であることを明らかにしました(PubMed)。
RNA結合タンパク質であるRoquinは,Regnase-1と共に炎症性サイトカインをはじめとした炎症に関連するタンパク質をコードするmRNAを分解し免疫系を制御することが知られていたが,これまでRegnase-1とRoquinの関係性についてはわかっていませんでした。我々は,Regnase-1とRoquinは時空間的に異なる分子機構により共通のmRNAの分解を制御することを明らかにしました(PubMed)。すなわち,Regnase-1とRoquinが共通したmRNAを異なる分子機構により分解することにより,炎症に関連するタンパク質の発現を厳密に制御していることが明らかになりました。更に,Regnase-1とRoquinによるT細胞活性化制御について検討したところ,Regnase-1とRoquinはそれぞれ個別にTh1分化を制御し,また心臓における炎症と線維化を抑制することを解明しました(PubMed)。
更に,Regnase-1は免疫制御だけでなく,鉄代謝も制御していることを解明しました(PubMed)。Regnase-1はPHD3 mRNAを分解することで,鉄代謝において重要な転写因子であるHIF2αを安定化させ,腸管での鉄吸収を促進する役割があることを明らかにしました。
今後,炎症のRNA結合タンパク質による調節メカニズムに関し,更に解析していくと共に炎症性疾患の制御法の開発にもつなげていきたいと考えています。
代表的な発表論文
- Cui, X., Mino, T., Yoshinaga, M., Nakatsuka, Y., Hia, F., Yamasoba, D., Tsujimura, T., Tomonaga, K., Suzuki, Y., Uehata, T., Takeuchi, O. (2017). Regnase-1 and Roquin Nonredundantly Regulate Th1 Differentiation Causing Cardiac Inflammation and Fibrosis. J. Immunol. 199, 4066-4077.
- Yoshinaga, M., Nakatsuka, Y., Vandenbon, A., Ori, D., Uehata, T., Tsujimura, T., Suzuki, Y., Mino, T., Takeuchi, O. (2017). Regnase-1 maintains iron homeostasis via the degradation of transferrin receptor 1 and prolyl hydroxylase domain-containing protein 3 mRNAs. Cell Reports 19, 1614-1630.
- Mino, T., Murakawa, Y., Fukao, A., Vandenbon, A., Wessels, H.-H., Ori, D., Uehata, T., Tartey, S., Akira, S., Suzuki, Y., Vinuesa, C.G., Ohler, U., Standley,D.M., Landthaler, M., Fujiwara, T., Takeuchi, O. (2015). Regnase-1 and Roquin Regulate a Common Element in Inflammatory mRNAs by Spatiotemporally Distinct Mechanisms. Cell 161, 1058-1073.
- Uehata, T., Iwasaki, H., Vandenbon, Matsushita, K., Cuellar, E.H., Kuniyoshi, K., Satoh, T., Mino, T., Suzuki, Y., Standley, D.M., Tsujimura, T., Rakugi, H., Isaka, Y., Takeuchi, O., Akira, S. (2013). Malt1-Induced Cleavage of Regnase-1 in CD4+ Helper T Cells Regulates Immune Activation. Cell 153, 1036-1049.
- Iwasaki, H., Takeuchi, O.*, Teraguchi, S., Matsushita, K., Uehata, T., Kuniyoshi, K., Satoh, T., Saitoh, T., Matsushita, M., Standley, D.M., Akira, S.* (*correspondence). (2011). The IκB kinase complex regulates the stability of cytokine-encoding mRNA induced by TLR-IL-1R by controlling degradation of regnase-1. Nat. Immunol. 12, 1167-1175.
- *Matsushita, K., *Takeuchi, O., Standley, D.M., Kumagai, Y., Kawagoe, T., Miyake, T., Satoh, T., Kato, H., Tsujimura, T., Nakamura, H., Akira, S. (*Equal contribution). (2009). Zc3h12a is an RNase essential for controlling immune responses by regulating mRNA decay. Nature 458, 1185-1190.
Takeuchi Lab.竹内研究室
〒606-8501
京都市左京区吉田近衛町
京都大学大学院医学研究科
医学専攻分子生体統御学講座
医化学分野
医学部A棟207号室
E-mail:otake @ mfour.med.kyoto-u.ac.jp
(@前後のスペースを除いて下さい)
TEL: 075-753-9500
FAX: 075-753-9502
大学院生・学振PD募集中!
竹内研究室では,修士課程・博士課程の入学希望の学生を広く募集しています。
また,学振PDも募集しています。
興味のある方はお気軽にご連絡下さい。
詳しくはこちら。